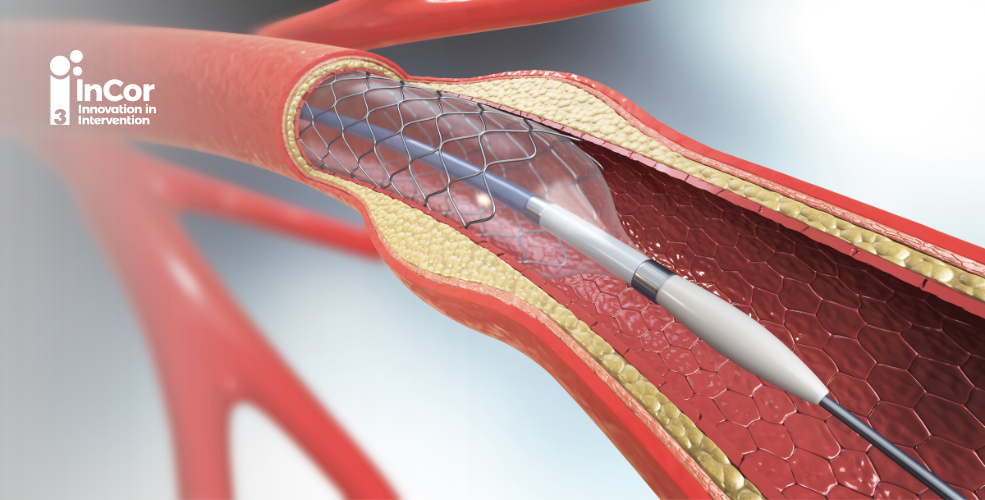
Short DAPT com clopidogrel após ICP?
Dra. Luhanda Monti

Após a realização de uma intervenção coronariana percutânea (ICP) com stent farmacológico (SF), a dupla terapia antiplaquetária (DAPT) se torna imperativa para prevenir trombose de stent e eventos cardiovasculares. No entanto, até 40% dos pacientes possuem alto risco de sangramento. Na última década o tempo DAPT após uma ICP com SF tem sido extensivamente discutido em função das novas plataformas de stent, que possuem menor risco trombótico, bem como a ascensão de inibidores P2Y12 mais potentes. A esse respeito, diversos estudos testaram diferentes esquemas de abreviação da DAPT, geralmente entre 1 e 3 meses, utilizando inibidores P2Y12 mais potentes, como o ticagrelor e prasugrel, tanto em pacientes crônicos, quanto agudos, que foram submetidos a ICP com SF, trazendo resultados satisfatórios, a depender do risco de sangramento vs. trombótico. Todavia, restava saber como seriam os resultados com o clopidogrel, haja vista seu amplo uso na prática clínica. Foi neste cenário que se iniciou a saga de trails STOPDAP-2. No presente artigo, trago uma análise crítica do primeiro ano de seguimento.
STOPDAPT-2 2019 JAMA – Seguimento de 01 ano
Trata-se de um ensaio clínico randomizado (ECR) de não inferioridade, que se prestou a avaliar a não-inferioridade da DAPT com aspirina (AAS) e clopidogrel por 1 mês, seguida de monoterapia com clopidogrel Vs. DAPT por 12 meses, com relação aos desfechos cardiovasculares e de sangramento, em pacientes submetidos à ICP.
Desenho:
ECR, multicêntrico em 90 hospitais no Japão, de não-inferioridade, placebo controlado, cujas análises foram conduzidas com o princípio de intention to treat. N=3045 pacientes / Seguimento médio: de 12 meses
Os pacientes submetidos a ICP foram randomizados para
1 mês de DAPT 🡪 CLOPIDOGREL por 12 meses (1.523)
12 meses de DAPT 🡪 AAS+ CLOPIDOGREL por 12 meses (n = 1.522)
Critérios de inclusão:
- Pacientes com doença arterial coronária (DAC) crônica ou síndrome coronária aguda (SCA) submetidos a ICP com SF cromo-cobalto eluído em everolimus.
Critério de exclusão:
- Necessidade de anticoagulação oral
- Uso de outro antiagregante plaquetário que não fosse AAS ou inibidor P2Y12
- Intolerância ao clopidogrel
- História de hemorragia intracraniana
Baseline:
-
- Idade média: 68 anos
- Mulheres: 21%
- Diabetes: 39%
- Doença arterial coronariana estável: 62%
- SCA: 37,7%
Desfecho composto primário: Morte cardiovascular (CV), infarto agudo do miocárdio (IAM) e acidente vascular cerebral (AVC)- isquêmico ou hemorrágico, trombose de stent e sangramento maior ou menor por TIMI.
Desfecho composto secundário: Componentes individuais do desfecho composto primário.
Resultados:
O desfecho primário de morte, IAM, trombose de stent, AVC, sangramento TIMI maior/menor em 1 ano, ocorreu em 2,4% do grupo de DAPT por 01 mês em Vs. 3,7% no grupo de DAPT por 12 meses p. não-inferioridade<0,001 (p. para superioridade = 0,04).
Resultados secundários:
-
- Morte, IAM, trombose de stent ou AVC em 1 ano: 2,0% do grupo DAPT de 1 mês em comparação com 2,5% do grupo TAPD de 12 meses (p para não inferioridade = 0,005)
- Sangramento maior/menor por TIMI em 1 ano: 0,4% do grupo DAPT de 1 mês em comparação com 1,5% do grupo DAPT de 12 meses (p para superioridade = 0,004);
- Apenas sangramento maior: DAPT 1 mês: 0,2 vs. DAPT 12 meses: 1,07 (p. de superioridade de 0,01)
- Bleeding Academic Research Consortium (BARC) 3 ou 5 – sangramento em 1 ano: 0,5% do grupo DAPT de 1 mês comparado com 1,8% do grupo TAPD de 12 meses (p para superioridade = 0,003).
- Trombose de stent definitiva ou provável: 0,3% do grupo DAPT 1 mês Vs. 0,07% do grupo DAPT por 12 meses (p para superioridade = 0,21)
Conclusão: Em pacientes submetidos à ICP com SF eluído em everolimus, a DAPT (AAS+ Clopidogrel) por 01 mês seguida de monoterapia com clopidogrel por 01 ano, foi não inferior à DAPT por 12 meses para eventos cardiovasculares isquêmicos e superior quanto a redução de sangramento.
Comentários sobre a aplicação prática
A DAPT por 01 mês seguida de monoterapia com clopidogrel proporcionou um benefício líquido para os eventos cardiovasculares e hemorrágicos, impulsionado por uma redução significativa de eventos hemorrágicos sem aumento de eventos isquêmicos, quando comparada ao esquema de DAPT 12 meses.
Nesse momento, você pensa: Então posso fazer short dapt por um mês e seguir com clopidogrel apenas? Bom pessoal, ao aplicarmos este ou qualquer resultado de ECR à nossa prática, uma análise pormenorizada se faz necessária. Estudos de não-inferioridade devem ser interpretados com cautela, pois possuem nuances que os diferem dos estudos de superioridade.
🡪 O primeiro ponto é identificar a margem de não-inferioridade, que traduz o quanto se “aceita” que a nova terapia seja inferior a padrão, pois o fato de x droga ser não-inferior, não é o mesmo que dizer que são equivalentes. O STOPDAPT-2 teve 2,3% de margem de não-inferioridade, correspondendo a 50% da taxa estimada de eventos, estando, portanto, adequado.
🡪 Segundo ponto: Se atente ao tipo de análise. Diferentemente dos estudos de superioridade, em ECR de não-inferioridade, a análise intention-to-treat pode favorecer o grupo intervenção a depender do percentual de cross-over, fazendo com que pareça não haver diferença entre o tratamento padrão e o novo a ser testado, ou seja, fazendo o estudo ser positivo, sem que isso seja verdadeiro, portanto, em estudos de não-inferioridade, a análise per-protocol é mais adequada. Neste STOPDAP-2 embora a análise tenha sido por intention-to-treat, os autores também analisaram per protocol. A análise de não- inferioridade per protocol foi condizente com a análise intention-to-treat para o desfecho primário estando, portanto, adequada.
🡪 Finalmente, com relação ao baseline, notem que foram incluídos tanto pacientes com SCA, quanto com DAC crônica, sendo esta última, a maioria. Sabemos que estas são doenças fisiopatologicamente distintas e que a SCA traz consigo maior risco trombótico. Houve um aumento numérico de trombose de stent e IAM no grupo DAPT 01 mês. Posteriormente, o estudo STOP DAPT-2 ACS realizado apenas com pacientes agudos, testou DAPT 1-2 meses com AAS + clopidogrel vs. clopidogrel, mostrou redução de sangramento com Short DAPT, contudo, não atendeu aos critérios de não-inferioridade para os desfechos isquêmicos, além de mostrar uma tendência no aumento de IAM e trombose de stent. Além disso, a mediana do SYNTAX Score foi de 9, o que traduz uma população de baixa complexidade anatômica e talvez de menor risco trombótico. De fato, trata-se de uma população de risco trombótico e hemorrágico baixo ou intermédio, com base na pontuação de risco CREDO-Kyoto (92% e 93%, respetivamente) e de PARIS (86% e 80%, respetivamente).
Em suma, a mensagem final é de que a ICP com SF de nova geração, no contexto da DAC crônica, a DAPT por 1 mês seguida com clopidogrel, ao invés de 6 meses como mandam as diretrizes, pode ser uma opção plausível em pacientes de maior risco de sangramento, desde que o risco trombótico seja baixo. Já no cenário da SCA, como o risco isquêmico permanece elevado até 1 ano após o evento, sendo inclusive bem maior nos primeiros meses, até o momento, seguimos as recomendações de diretrizes, que orientam, manter DAPT por 12 meses como regra geral. A abreviação da DAPT neste cenário, deve ser individualizada em casos de alto risco de sangramento, pautada no tipo de stent e fármaco eluidor, bem como no tipo de IP2Y12 empregado.
Referências:
Watanabe H, Domei T, Morimoto T, et al. Effect of 1-Month Dual Antiplatelet Therapy Followed by Clopidogrel vs 12-Month Dual Antiplatelet Therapy on Cardiovascular and Bleeding Events in Patients Receiving PCI: The STOPDAPT-2 Randomized Clinical Trial. JAMA 2019;321:2414-27.
Watanabe H, Morimoto T, Natsuaki M,et al. STOPDAPT-2 ACS Investigators. Comparison of Clopidogrel Monotherapy After 1 to 2 Months of Dual Antiplatelet Therapy With 12 Months of Dual Antiplatelet Therapy in Patients With Acute Coronary Syndrome: The STOPDAPT-2 ACS Randomized Clinical Trial. JAMA Cardiol. 2022 Apr 1;7(4):407-417.

 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention
 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention
 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention
 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention
 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention
 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention