Fundamentos em Síndrome Coronária Aguda: tudo o que você precisa saber sobre complicações pós-infarto agudo do miocárdio – Episódio 5: Trombo em ventrículo esquerdo
Dr Cesar Augusto Caporrino Pereira

Introdução
A formação de trombo em ventrículo esquerdo (VE) é uma complicação reconhecida após o infarto agudo do miocárdio (IAM), especialmente em pacientes com infartos extensos da parede anterior. Apesar dos avanços nas estratégias de reperfusão e no tratamento farmacológico contemporâneo, o trombo ventricular permanece clinicamente relevante devido ao risco de eventos embólicos sistêmicos, particularmente acidente vascular cerebral. O reconhecimento precoce, diagnóstico adequado e manejo terapêutico apropriado são fundamentais para reduzir a morbidade associada a essa condição.
Epidemiologia
A incidência de trombo ventricular esquerdo após IAM varia conforme diversos fatores, incluindo extensão do infarto, território acometido, método de imagem utilizado e estratégia de reperfusão empregada. Estima-se incidência aproximada de 17% dos infartos, sendo mais frequente em infartos anteriores. Eventos embólicos podem ocorrer em até 16% dos pacientes durante seguimento de cinco anos. Estratégias de reperfusão (angioplastia primária, fibrinólise e cirurgia de revascularização miocárdica), medicações para insuficiência cardíaca e antiagregantes potentes, reduziram a incidência dessa complicação (figura 1).
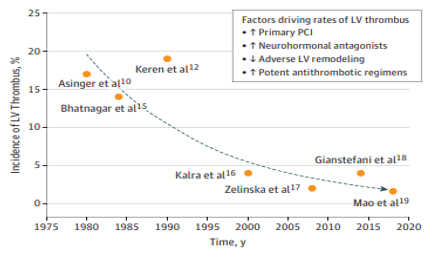
Figura 1: Queda na incidência da formação de trombo em VE ao longo dos anos.
Fisiopatologia
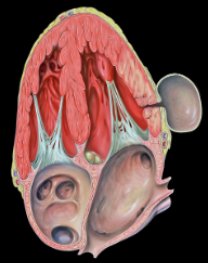
A formação do trombo ventricular esquerdo está relacionada à tríade de Virchow: estase sanguínea, lesão endotelial e estado pró‑trombótico. Após infartos extensos, especialmente anteriores, ocorrem alterações regionais da contratilidade ventricular, como hipocinesia, acinesia ou discinesia apical. Essas alterações favorecem estase sanguínea e ativação de cascatas trombogênicas, criando ambiente propício à formação de trombos no VE.
Diagnóstico
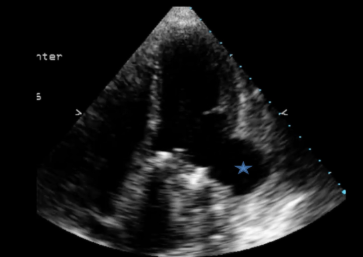
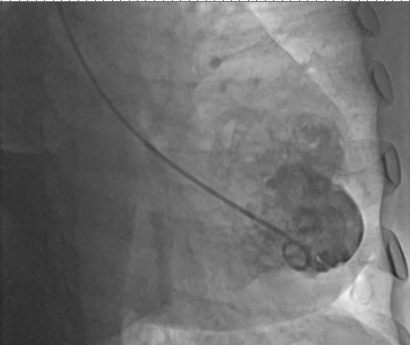
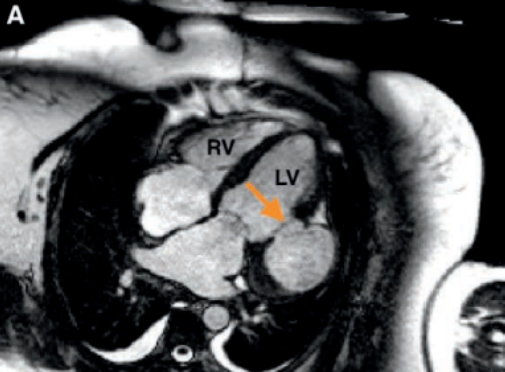
A maioria dos trombos se forma nas primeiras duas semanas após o infarto, sendo que cerca de 90% surgem nesse período. O ecocardiograma transtorácico é o método diagnóstico inicial mais utilizado, permitindo avaliação da função ventricular e detecção do trombo. O ecocardiograma com contraste aumenta a sensibilidade diagnóstica. A ressonância magnética cardíaca apresenta maior sensibilidade e especificidade, sendo considerada método de referência para identificação e caracterização do trombo ventricular esquerdo (figura 2).
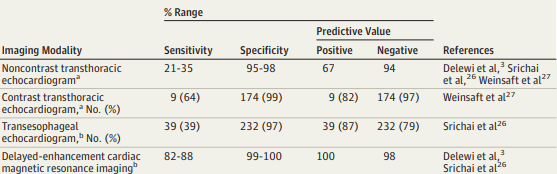
Figura2: Comparativo entre os principais métodos diagnósticos para trombo em VE.
Prevenção e Tratamento
Estudos realizados na era pré‑reperfusão sugeriram que anticoagulação poderia reduzir formação de trombos e eventos embólicos após infarto anterior. Entretanto, evidências iniciais apresentavam limitações metodológicas principalmente quanto à segurança. Estudos posteriores avaliaram a anticoagulação como forma de prevenção à formação de trombo, sem demonstrar redução significativa em reinfarto ou mortalidade, havendo redução da formação de trombo, porém aumento de sangramento.
Anticoagulação
O tratamento do trombo ventricular esquerdo baseia‑se tradicionalmente na anticoagulação oral com antagonistas da vitamina K, especialmente varfarina. Mais recentemente, anticoagulantes orais diretos (DOACs) vêm sendo utilizados como alternativa terapêutica. O manejo torna‑se mais complexo no cenário pós‑infarto, no qual pacientes frequentemente recebem dupla antiagregação plaquetária, aumentando o risco de sangramento e exigindo avaliação individualizada.
DOAC vs Varfarina
Estudos recentes comparando DOACs com antagonistas da vitamina K sugerem eficácia semelhante em termos de resolução do trombo e prevenção de eventos embólicos. Em meta-análises (figura 3) trials recentes como o RIVAWAR (figura 4), não foram observadas diferenças significativas em mortalidade, acidente vascular cerebral isquêmico ou sangramento maior.
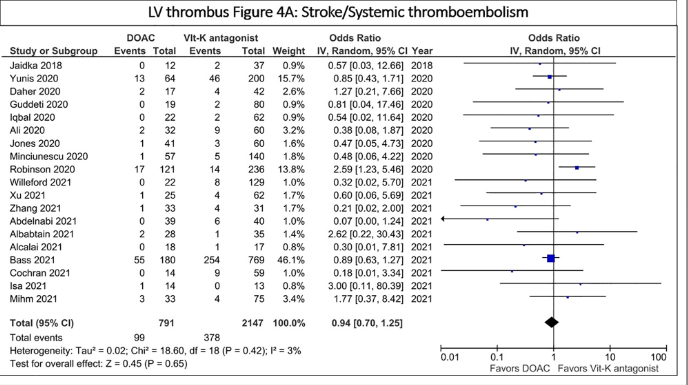
Figura 3: Meta-análise comparando DOAC vs varfarina em contexto de trombo em VE.
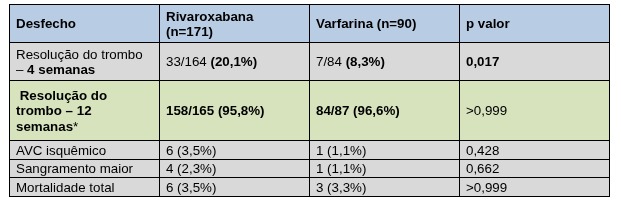
Figura 4: Tabela de resultados do estudo RIVAWAR . *Desfecho primário do estudo
O estudo RIVAWAR avaliou a eficácia e segurança da rivaroxabana em comparação à varfarina no tratamento do trombo em ventrículo esquerdo após infarto do miocárdio. Trata-se de um ensaio clínico randomizado, aberto, de não inferioridade, que incluiu 261 pacientes com trombo ventricular esquerdo confirmado, sendo 171 tratados com rivaroxabana e 90 com varfarina. No desfecho precoce em 4 semanas, a taxa de resolução do trombo foi numericamente maior no grupo rivaroxabana, sugerindo resolução mais precoce do trombo quando comparada à varfarina. Já no desfecho primário em 12 semanas, que avaliou a resolução do trombo ventricular esquerdo, os resultados foram semelhantes entre rivaroxabana e varfarina, confirmando a não inferioridade da rivaroxabana nesse contexto.
No protocolo do estudo, os pacientes permaneceram em dupla antiagregação plaquetária com ácido acetilsalicílico e clopidogrel por 1 mês e mais dois meses com clopidogrel. A rivaroxabana foi utilizada na dose de 20 mg uma vez ao dia, durante o período de tratamento e acompanhamento do trombo por 12 semanas. Esses resultados sugerem que os anticoagulantes orais diretos podem representar uma alternativa terapêutica viável aos antagonistas da vitamina K no manejo do trombo ventricular esquerdo pós-infarto.
Manejo
Na Figura 5 é apresentada uma proposta de abordagem para a condução do paciente após infarto agudo do miocárdio em relação à investigação e ao manejo do trombo em ventrículo esquerdo. É importante ressaltar que, uma vez identificado trombo em ventrículo esquerdo, a anticoagulação está indicada independentemente de sua morfologia, incluindo os trombos murais. Isso se justifica pelo fato de que trombos murais podem ser responsáveis por até cerca de 40% dos eventos tromboembólicos, reforçando a necessidade de tratamento anticoagulante nesses pacientes.
Na tomada de decisão terapêutica, é fundamental realizar sempre que possível avaliação individualizada do risco trombótico e do risco de sangramento, uma vez que o equilíbrio entre esses fatores orienta tanto a duração da anticoagulação quanto a combinação com terapias antiplaquetárias. Grande parte das estratégias atualmente utilizadas para a associação entre anticoagulação e antiagregação plaquetária deriva de evidências provenientes de estudos em pacientes com fibrilação atrial submetidos à intervenção coronária percutânea, como os ensaios AUGUSTUS, RE-DUAL PCI, PIONEER AF-PCI, WOEST e ENTRUST-AF PCI.
A partir dessas evidências, particularmente de análises adicionais do estudo AUGUSTUS, consolidou-se o conceito de que o período de terapia tripla — composto por ácido acetilsalicílico, clopidogrel (ou eventualmente ticagrelor, devendo-se evitar o uso de prasugrel) e um anticoagulante oral direto (DOAC) — deve ser o mais curto possível, idealmente limitado a no máximo um mês. Em pacientes com alto risco de sangramento, pode-se considerar a suspensão precoce do AAS ainda durante a hospitalização, mantendo-se dupla terapia com clopidogrel e DOAC.
Após esse período inicial, recomenda-se a manutenção da dupla terapia por um período que geralmente varia entre seis e doze meses, seguido posteriormente pela manutenção isolada da anticoagulação oral, estratégia apoiada por estudos como AFIRE, AQUATIC e EPIC-CAD, nos quais pacientes com fibrilação atrial constituem a totalidade ou a maioria das populações estudadas.
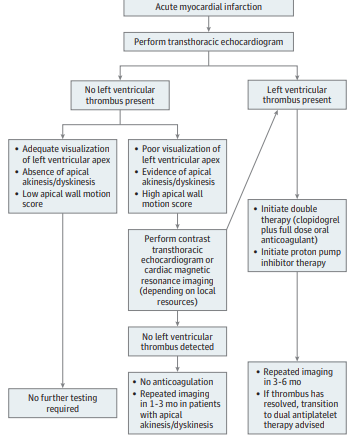
Figura 5: Sugestão de manejo do paciente em pós-IAM (McCarthy CP; JAMA Cardiol, 2018).
Caso haja a manutenção do trombo após anticoagulação de 3 a 6 meses devemos avaliar caso a caso, tendo como opção alteração do esquema de anticoagulação (varfarina por DOAC, alterar DOAC de diferente mecanismo de ação) ou até suspender anticoagulação Figuras 6 e 7.
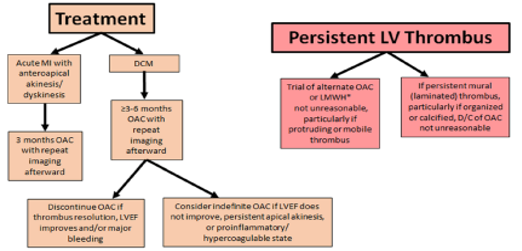
Figura 6: Revisão (Levine GN; Circulation, 2022) nos apresenta algoritmo de manejo do trombo em ventrículo esquerdo, tanto no cenário pós-IAM quanto nas cardiomiopatias dilatadas, inclui diferentes estratégias terapêuticas e possibilidades de ajuste do tratamento. Nos casos de persistência do trombo, podem ser consideradas alternativas como a modificação do regime de anticoagulação ou, em situações selecionadas e após reavaliação clínica e por imagem, a eventual suspensão da terapia anticoagulante.
LMWH: heparina de baixo peso molecular
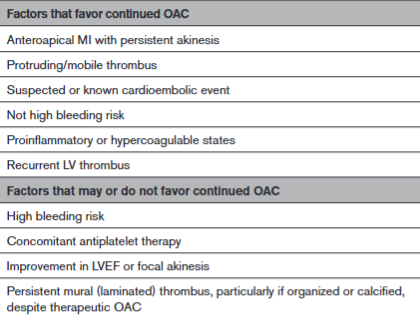
Figura 7: Fatores para avaliar continuação ou suspensão da anticoagulação em trombos de VE persistentes.
Diretrizes
As diretrizes atuais recomendam anticoagulação para o tratamento do trombo em ventrículo esquerdo confirmado após infarto agudo do miocárdio (Figura 8). Entretanto, a utilização de anticoagulação com finalidade profilática permanece um tema de debate. Algumas revisões sobre o assunto, como o documento de Levine GN et al., publicado na Circulation em 2022, que fundamenta recomendações posteriormente incorporadas na diretriz da American Heart Association de 2025 para Síndrome Coronariana Aguda, discutem a possibilidade de anticoagulação profilática em situações selecionadas. Nesses cenários, a decisão deve ser individualizada, considerando-se o risco de formação de trombo ventricular esquerdo — particularmente na presença de acinesia ou discinesia apical após infarto anterior — e o risco de sangramento associado à terapia antitrombótica.
Um ensaio clínico (Zhang Z., JACC Cardiovasc Interv. 2022) randomizado, aberto e unicêntrico, com 279 pacientes, avaliou se a adição de rivaroxabana em baixa dose (2,5 mg duas vezes ao dia por 30 dias) à dupla antiagregação plaquetária (clopidogrel ou ticagrelor) poderia reduzir a formação de trombo em ventrículo esquerdo após IAM. O estudo demonstrou redução significativa na incidência de trombo ventricular em comparação com DAPT isolada (0,7% vs 8,6%; HR 0,08; IC95% 0,01–0,62), sem aumento de sangramento. Entretanto, os resultados devem ser interpretados com cautela devido a limitações metodológicas, incluindo desenho aberto, realização em centro único, elevada taxa de perda de seguimento (16,5%) e predominância de pacientes com fração de ejeção >45%.

Figura 8: Recomendações da diretriz da ESC de Síndome Coronariana Aguda de 2023.
Conclusão
O trombo ventricular esquerdo permanece uma complicação relevante do infarto agudo do miocárdio, particularmente em pacientes com infartos anteriores extensos e disfunção ventricular significativa. O diagnóstico precoce por métodos de imagem adequados é essencial para reduzir o risco de eventos embólicos. A anticoagulação permanece a base do tratamento, com crescente evidência apoiando o uso de anticoagulantes orais diretos em pacientes selecionados.
Referências:
- McCarthy CP, Murphy S, Venkateswaran RV, et al. Left ventricular thrombus after acute myocardial infarction. JAMA Cardiol. 2018.
- Visser CA, Kan G, Lie KI, et al. Left ventricular thrombus following acute myocardial infarction: a prospective serial echocardiographic study. Eur Heart J. 1983.
- Levine GN, McEvoy JW, Fang JC, et al. Management of left ventricular thrombus. Circulation. 2022;146:e205–e223.
- Vaitkus PT, Barnathan ES. Embolic potential, prevention and management of mural thrombus complicating anterior myocardial infarction: a meta-analysis. J Am Coll Cardiol. 1993;22:1004–1009.
- Kontny F, et al. Randomized trial of low molecular weight heparin in prevention of left ventricular thrombus formation after anterior myocardial infarction. J Am Coll Cardiol. 1997;30:962–969.
- Bangalore S. Anticoagulation for left ventricular thrombus. Eur Heart J. 2024.
- Zhang Z, et al. Prophylactic rivaroxaban therapy for left ventricular thrombus after anterior ST-segment elevation myocardial infarction. JACC Cardiovasc Interv. 2022.
- Lemesle G, et al. Aspirin in patients with chronic coronary syndrome receiving oral anticoagulation. N Engl J Med. 2025.
- Yasuda S, et al. Antithrombotic therapy for atrial fibrillation with stable coronary disease. N Engl J Med. 2019;381:1103–1113.
Assista ao vídeo



 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention
 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention

 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention
