Dra. Luhanda Leonora Cardoso Monti Sousa
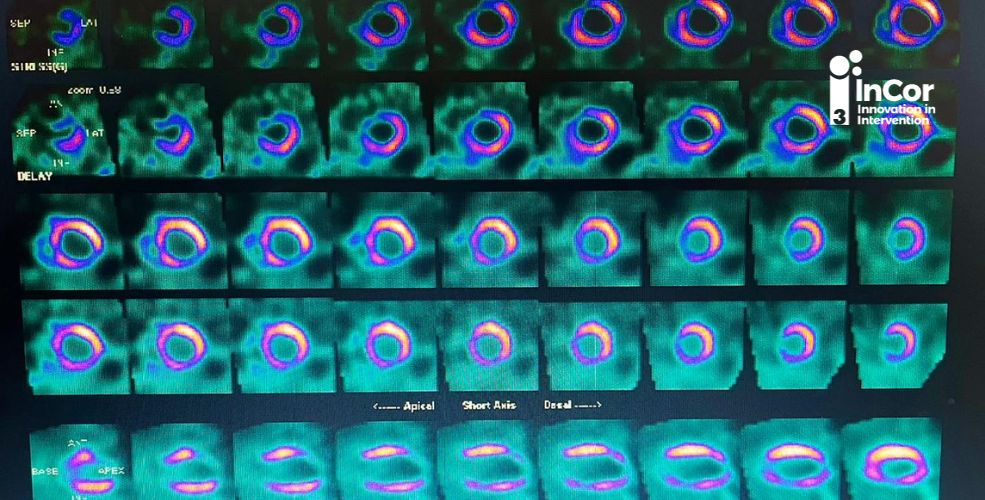
Por muito tempo a presença de isquemia ≥ 10%, foi utilizada como ponto a partir do qual, a revascularização miocárdica estaria indicada para melhora de prognóstico, a despeito das evidências oriundas de estudos observacionais e sub análises de ensaios clínicos randomizados (ECR). O principal estudo a sustentar as recomendações de diretrizes foi o Hachamovitch 2, um estudo observacional que, segundo os autores, foi projetado para “imitar” um ECR através do escore de propensão.
A conclusão foi que o aumento da carga isquêmica (entre 0 a 10-12,5%) se associou à maior probabilidade de cirurgia de revascularização miocárdica (CRM), que por sua vez, melhorou a sobrevida na presença de isquemia moderada (≥ 10%) à importante (≥ 20%), quando comparada à terapia médica otimizada (TMO) isolada. Contudo, uma análise minuciosa, mostra uma série de imperfeições metodológicas. Este foi um estudo observacional, logo, os grupos eram heterogêneos e não comparáveis (> 9000 pacientes na TMO e 671 no braço CRM). Além disso, não se sabe se todos os pacientes tinham doença arterial coronária (DAC) epicárdica, visto a ausência de dados sobre a anatomia coronária e o conhecimento atual acerca de outras causas para isquemia.
No estudo COURAGE, que comparou ICP vs.TMO em pacientes com DAC estável e pelo menos 1 lesão ≥ 70% com isquemia presente ou ≥ 80% sem isquemia, não houve diferença para sobrevida entre as duas estratégias. Um subestudo do COURAGE, envolvendo 314 pacientes com teste perfusional seriado (antes do tratamento e 6 e 18 meses) reportou que a redução ≥5% de isquemia nos pacientes submetidos à ICP, partindo de uma isquemia basal moderada a grave, se correlacionou à menor mortalidade CV e IAM no modelo não ajustado (p= 0,001), mas sem significância no modelo ajustado ao risco (p=0,08). A despeito da ausência de benefício estatisticamente significante na análise multivariada, os autores chegaram a sugerir uma redução de isquemia residual ≥ 5% como meta terapêutica. Nesse contexto, a isquemia ≥ 10% foi o ponto de corte sugerido pelo estudo COURAGE, para o qual, a revascularização traria benefício líquido.
A rápida ascensão da cardiologia intervencionista nos trouxe o FFR (Fractional Flow Reserve), uma forma de se avaliar a funcionalidade de lesões intermediárias, que usa a diferença de pressão de perfusão sob hiperemia máxima, podendo-se inferir isquemia. Os resultados do FAME-2 mostraram redução no desfecho primário (revascularização não planejada morte por todas as causas e IAM não fatal) em pacientes com DAC estável e lesões ≥ 50% com FFR ≤ 0,80 vs. TMO. Desde então, as diretrizes americanas e europeias de revascularização, advogam o uso do FFR para guiar a tomada de decisão da ICP em lesões moderadas com classe I de recomendação.
Com a premissa de responder a todas essas questões, o ISCHEMIA trial se propôs a avaliar se uma estratégia invasiva inicial com cinecoronariografia (CINE) e revascularização quando factível, seria superior à conservadora inicial em pacientes com teste isquêmico não invasivo de alto risco ( isquemia ≥ 10%), excluindo lesão de TCE ≥ 50%, com angiotomografia de artérias coronárias (angio TCC), FE ≤ 35% e angina limitante. No seguimento de 3,2 anos, os autores concluíram que a estratégia invasiva não reduziu o desfecho primário composto, mesmo na vigência de DAC multiarterial e acometimento de artéria descendente anterior (ADA) proximal. A observação de que o grupo intervenção teve menores taxas de IAM espontâneo aos 4 anos e melhora na qualidade de vida inferida pelo controle de angina em posterior subanálise, é de suma importância para individualização de casos na vida real. Mais recentemente com mediana de seguimento de 5,2 anos, o ISCHEMIA EXTEND, mostrou menores taxas de morte CV 6,4% no grupo intervenção vs. TMO 8,6% (p = 0,008), mas este benefício foi diluído pelo aumento de mortalidade não cardiovascular (infecção e neoplasia) no grupo intervenção 4,4% vs. 5,5% TMO (p = 0,016), sem apresentar, no entanto, diferença em morte global. Algo já questionado, mas que ainda não obtivemos resposta. A ausência de associação entre o grau de isquemia e mortalidade por todas as causas (p para tendência = 0,33), bem como IAM (p para tendência = 0,04) e a forte associação entre DAC mais extensa (escore de Duke modificado) com mortalidade por todas as causas (p para tendência < 0,001) e IAM (p para tendência < 0,001), vai de encontro ao fato de que a anatomia parece ser um preditor mais fidedigno de DAC de alto risco do que a isquemia.
A diretriz americana de revascularização miocárdica 2021 ACC/AHA/SCAI Coronary Revascularization, parece ter incorporado os resultados do ISCHEMIA, não mais indicando revascularização baseada na extensão de isquemia para melhora de sobrevida, como fez a ESC em 2019. Além disso, fez um “downgrade” para IIb na recomendação de revascularização para melhora de sobrevida global e IIa para redução de morte CV e IAM, em pacientes multiarterias.
Atualmente, a isquemia não deve ser utilizada de forma isolada para guiar revascularização por prognóstico, ao contrário, pode ser agregada a outras variáveis de forma individualizada, sobretudo nas discussões de Heart Team.
Embora seja um marcador de gravidade, as decisões acerca da revascularização miocárdica ficam a cargo da anatomia (burden aterosclerótico) e função ventricular.
Referências
1. Neumann FJ, Sousa-Uva M, Ahlsson A, Alfonso F, Banning AP, Benedetto U, et al. 2018 ESC/EACTS guidelines on myocardial revascularization. Eur Heart J. 2019 Jan;40(2):87–165. https://doi. org/10.1093/eurheartj/ehy394
2. Lawton JS, Tamis-Holland JE, Bangalore S, Bates ER, Beckie TM, Bischoff JM, et al. 2021 ACC/ AHA/SCAI guideline for coronary artery revas- cularization: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Cir- culation. 2022 Jan;145(3):e18–114.
3. MaronDJ, HochmanJS, ReynoldsHR, Bangalore S, O’Brien SM, Boden WE, et al. Initial invasive or conservative strategy for stable coronary disease. N Engl J Med. 2020;382(15):1395–407. https:// doi.org/10.1056/NEJMoa1915922
4. Windecker S, Stortecky S, Stefanini GG et al.; Revascularisation versus medical treatment in patients with stable coronary artery disease: network meta-analysis. BMJ. 2014 Jun 23;348: g3859.
5. Xaplanteris P, Fournier S, Pijls NHJ et al.; FAME 2 Investigators. Five-Year Outcomes with PCI Guided by Fractional Flow Reserve. N Engl J Med. 2018 Jul 19;379(3):250-259.
6. Weintraub WS, Spertus JA, Kolm P et al.; COURAGE Trial Research Group, Mancini GB. Effect of PCI on quality of life in patients with stable coronary disease. N Engl J Med. 2008;359(7):677-87.
7. Hueb W, Lopes N, Gersh BJ et al.; Ten-year follow-up survival of the Medicine, Angioplasty, or Surgery Study (MASS II): a randomized controlled clinical trial of 3 therapeutic strategies for multivessel coronary artery disease. Circulation. 2010;122(10):949-57.
8. Mohr FW, Morice MC, Kappetein AP et al.; Coronary artery bypass graft surgery versus percutaneous coronary intervention in patients with three-vessel disease and left main coronary disease: 5-year follow-up of the randomised, clinical SYNTAX trial. Lancet. 2013 Feb 23;381(9867):629-38.
9. Pijls NHJ, van Schaardenburgh P, Manoharan G, et al. Percutaneous coronary intervention of functionally non-significant stenosis: 5-year follow-up of the DEFER study. J Am Coll Cardiol 2007;49:2105–11
10. Hachamovitch R, Hayes SW, Friedman JD, et al. 2003. Comparison of the short-term survival benefit associated with revascularization compared with medical therapy in patients with no prior coronary artery disease undergoing stress myocardial perfusion single photon emission computed tomography. Circulation 107(23):2900–7.
11. Hachamovitch R, Rozanski A, Shaw LJ, et al. 2011. Impact of ischaemia and scar on the therapeutic benefit derived from myocardial revascularization versus medical therapy among patients undergoing stress-rest myocardial perfusion scintigraphy. Eur. Heart J. 32(8):1012–24
12. Boden WE, Stone PH. 2021. To stent or not to stent? Treating angina after ISCHEMIA—why a conservative approach with optimal medical therapy is the preferred initial management strategy for chronic coronary syndromes: insights from the ISCHEMIA trial. Eur. Heart J. 42(14):1394–40
13. 1. Sousa LLCM, Gowdak LHW. Tratamento invasivo: Bases para a decisão. Insuficiência Coronária Crônca. Rev Soc Cardiol Estado de São Paulo, 2022; 32(4): 460-466.INSS 2595-4644-Versão online.
14. Anthopolos R, Maron DJ, Bangalore S, Reynolds HR, Xu Y, O’Brien SM, Troxel AB, Mavromichalis S, Chang M, Contreras A, Hochman JS on behalf of ISCHEMIA-EXTEND Research Group. American Heart Journal. 2022 Oct 04.

 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention
 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention
 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention

