Novos Conceitos da Terapia Antiplaquetária Após Intervenções Coronárias Percutâneas
Luiz Mapa Santos | Carlos A.H.M. Campos
A utilização da terapia antiplaquetária na cardiologia remonta à década de 1950, quando a aspirina (AAS) começou a ser empregada. Nos últimos 30 anos, os avanços e evoluções dos stents impulsionaram a ampla adoção da terapia dupla antiplaquetária (DAPT), composta por AAS e um inibidor de P2Y12, como o padrão de cuidado. Recentemente, as estratégias de DAPT após intervenções coronárias percutâneas (ICP) têm passado por mudanças significativas em diversos parâmetros: medicamentos utilizados, suas doses e a duração da terapia. Essas alterações são baseadas em numerosos estudos clínicos desenvolvidos para acompanhar os avanços nas plataformas dos stents e para considerar os diferentes perfis de risco, tanto isquêmico quanto hemorrágico.
Frente ao surgimento de várias evidências que propõem diferentes estratégias antiplaquetárias para diversos tipos de paciente, o médico se vê imerso numa infinidade de termos como “short-DAPT, prolonged-DAPT, switch”, na ausência de uma padronização que permita fácil compreensão e torne a mudança de estratégia mais factível.
Capodanno et al, através do The Academic Research Consortium (ARC), propõem um consenso para homogeneizar a linguagem empregada nas estratégias antiplaquetárias. É proposto que a terapia antiplaquetária possa ser modificada de duas formas: reduzindo (descalonando) ou aumentando (escalonando) a intensidade da inibição plaquetária. Em cada uma das estratégias, a intensidade pode ser modificada por mudanças no tipo, dose ou número de drogas utilizados (Figura 1).
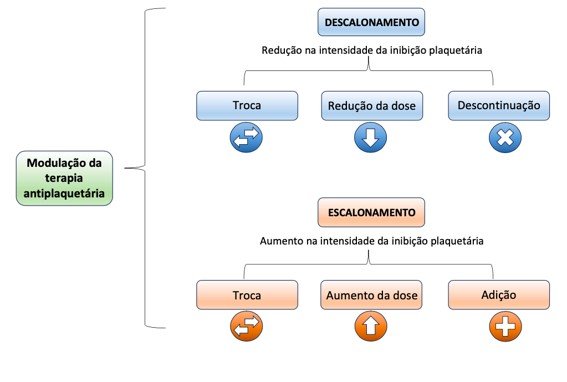
Figura 1: Estraégias para modulação da DAPT. Adaptado de Circulation. 2023;147:1933-1944.
O descalonamento do efeito antiplaquetário objetiva-se a reduzir o risco hemorrágico do paciente. São descritas modificações, no tipo, dose ou duração do regime duplo.
No que se refere à troca, podemos citar a troca do prasugrel ou ticagrelor pelo clopidogrel, que usualmente ocorre em pacientes após SCA que estão em uso de um dos inibidores mais potentes, como visto nos estudos TALOS-AMI e TOPIC.
O descalonamento pela redução da dose consiste na redução das doses do ticagrelor ou prasugrel, comparado à dose padrão. Existem dados limitados na literatura que validam a eficácia e segurança nessa estratégia de descalonamento, mas os existentes comparam o uso de prasugrel 5mg por dia (HOST-REDUCE-POLYTECH-ACS) e ticagrelor 60mg duas vezes ao dia (PEGASUS-TIMI 54 trial).
Já o descalonamento por descontinuação refere-se à interrupção do uso de 1 dos antiplaquetários, mantendo uso da AAS ou inibidor P2Y12 em monoterapia. As evidências atuais que abordam a descontinuação da DAPT, suportam a suspensão do inibidor P2Y12 ou AAS após 1 mês no contexto de DAC estável. No contexto de SCA, contemplam a suspensão do inibidor P2Y12 após 3 a 6 meses de DAPT ou no caso da suspensão do AAS, após 1 a 3 meses.
Por se tratar da estratégia que possui mais dados na literatura, as diretrizes mais recentes já contemplam o descalonamento por descontinuação com diferentes níveis de evidência e graus de recomendação. Existem evidências tanto para a suspensão do AAS (TICO trial, STOPDAPT-2 ACS) e do inibidor do P2Y12 (ONE-MONTH DAPT trial, SMART-DATE, REDUCE-ACS) sendo que os trials mais recentes como o MASTER-DAPT deixaram a escolha de qual suspender à critério do médico assistente do paciente, enfatizando mais o tempo de suspensão do que o tipo de droga suspensa.
O escalonamento da terapia plaquetária inclui as estratégias que objetivam reduzir o risco trombótico/isquêmico do paciente através do aumento do efeito antiplaquetário. Pode ser realizada pela troca, pelo aumento da dose ou adição de uma droga antiplaquetária.
O escalonamento pela troca usualmente refere-se à troca clopidogrel por um inibidor P2Y12 mais potente. Ocorre mais frequentemente em pacientes com DAC estável submetidos à angioplastia eletiva e tratados com clopidogrel, como terapia padrão. Existem dois trials que comparam esse escalonamento após ICPs eletivas (SASSICAIA e ALPHEUS), que não mostraram efetividade da estratégia. Apesar disso, existem dados que compravam eficácia da estratégia quando realizada de modo guiado por testes de função plaquetária (PATH-PCI). Por essa razão, essa estratégia é pouco abordada nas diretrizes e com baixo grau de recomendação, podendo ser considerada principalmente para pacientes com evidência de reatividade ao clopidogrel, genótipo de perda de função do CYP2C19 ou em situações de alto risco na angioplastia eletiva (por exemplo, implante de stent sub-ótimo, ICP complexa em TCE ou ICP multivasos).
No que se refere ao escalonamento por aumento de dose, podemos citar o aumento nas doses de clopidogrel ou AAS, estratégia que não é mencionada nas diretrizes atuais de DAC estável, uma vez que os estudos não mostraram bons resultados (CURRENT-OASIS 7, GRAVITAS, ADAPTABLE trial).
Sobre o escalonamento por adição, a estratégia compreende o emprego de uma segunda droga antiplaquetária em regimes de monoterapia. As estratégias para prolongamento do tempo de DAPT já são contempladas nas diretrizes baseando-se nos trials DAPT, PEGASUS-TIMI 54, THEMIS.
Portanto, à luz de diversas evidências que suportam diferentes estratégias de DAPT, o cardiologista deve ter em mente que os regimes antiplaquetários cada vez mais se tornam individualizados. As diretrizes algumas vezes contemplam tais estratégias, mas por tratar-se de um tema complexo e com significativos impactos em eventos cardiovasculares, a comunidade científica trabalha à todo vapor na geração de novas evidências. Escolher e empregar um regime antiplaquetário não deve seguir uma receita pronta. A definição deve ser individualizada e a padronização acima propõe uma esquematização para que o médico possa definir seu paciente, definir a estratégia para redução ou aumento da força de antiagregação e conhecer a evidência que suporta cada uma das estratégias.
Referências:
- Capodanno D, Mehran R, Krucoff MW, et al. Defining strategies of modulation of antiplatelet therapy in patients with coronary artery disease: a consensus document from the Academic Research Consortium. Circulation. 2023;147:1933-1944.
Thomas A, Gitto M, Shah S, et al. Antiplatelet Strategies Following PCI: A Review of Trials Informing Current and Future Therapies. Journal of the Society for Cardiovascular Angiography & Interventions, 2023; 2:3
Av. Dr. Enéas de Carvalho Aguiar, 44 | +55 (11) 2661.5310 | contato@triplei.com.br




 O Triple I - InCor Innovation in Intervention
O Triple I - InCor Innovation in Intervention


 O TRIPLE I - InCor Innovation in Intervention
O TRIPLE I - InCor Innovation in Intervention O TRIPLE I - InCor Innovation in Intervention
O TRIPLE I - InCor Innovation in Intervention